Статьи
Другий закон термодинаміки
Втор про е поч а ло термодін а мики, принцип, який встановлює незворотність макроскопічних процесів, що протікають з кінцевою швидкістю. На відміну від суто механічних (без тертя) або електродинамічних (без виділення Джоу-лівої теплоти) оборотних процесів , Процеси, пов'язані з теплообміном при кінцевій різниці температур (т. Е. Поточні з кінцевою швидкістю), з тертям, дифузією газів, розширенням газів в порожнечу, виділенням джоулева теплоти і т.д., незворотні, т. Е. Можуть мимовільно протікати тільки в одному напрямку (див. необоротні процеси ).
Історично В. н. т. виникло з аналізу роботи теплових машин (С. Карно , 1824). Існує кілька еквівалентних формулювань В. н. т. Сама назва «В. н. т. »і історично перша його формулювання (1850) належать Р. Клаузиусу : Неможливий процес, при якому теплота переходила б мимовільно від тіл більш холодних до тіл більш нагрітих. При цьому мимовільний перехід не слід розуміти у вузькому сенсі: неможливий не тільки безпосередній перехід, його неможливо здійснити і за допомогою машин або приладів без того, щоб в природі не сталося ще яких-небудь змін. Іншими словами, неможливо провести процес, єдиним наслідком якого був би перехід теплоти від більш холодного тіла до більш нагрітого. Якби (в порушення положення Клаузіуса) такий процес виявився можливим, то можна було б, розділивши один тепловий резервуар на 2 частини і переводячи теплоту з однієї в іншу, отримати 2 резервуара з різними температурами. Це дозволило б, в свою чергу, здійснити Карно цикл і отримати механічну роботу за допомогою періодично діючої (т. е. багато разів повертається до вихідного стану) машини за рахунок внутрішньої енергії одного теплового резервуара. Оскільки це неможливо, в природі неможливі процеси, єдиним наслідком яких був би підйом вантажу (т. Е. Механічна робота), вироблений за рахунок охолодження теплового резервуара (така формулювання В. н. Т., Дана У. Томсоном , 1851). Назад, якби можна було отримати механічну роботу за рахунок внутрішньої енергії одного теплового резервуара (в протиріччі з В. н. Т. По Томсону), то можна було б порушити і положення Клаузіуса. Механічну роботу, отриману за рахунок теплоти від більш холодного резервуара, можна було б використовувати для нагрівання більш теплого резервуара (наприклад, тертям) і тим самим здійснити перехід теплоти від холодного тіла до нагрітого. Обидві наведені формулювання В. н. т., будучи еквівалентними, підкреслюють істотну відмінність у можливості реалізації енергії, отриманої за рахунок зовнішніх джерел роботи, і енергії безладного (теплового) руху частинок тіла.
Можливість використання енергії теплового руху частинок тіла (теплового резервуара) для отримання механічної роботи (без зміни стану інших тіл) означала б можливість реалізації так званого вічного двигуна 2-го роду, робота якого не суперечила б закону збереження енергії. Так, робота двигуна корабля за рахунок охолодження забортної води океану - доступного і практично невичерпного резервуара внутрішньої енергії - не суперечить закону збереження енергії, але якщо, окрім охолодження води, ніде інших змін немає, то робота такого двигуна суперечить В. н. т. У реальному тепловому двигуні процес перетворення теплоти в роботу обов'язково пов'язаний з передачею певної кількості теплоти зовнішньому середовищі. В результаті теплової резервуар двигуна охолоджується, а більш холодна зовнішнє середовище нагрівається, що знаходиться в згоді зі В. н. т. Отже, В. н. т. можна формулювати і як неможливість вічного двигуна 2-го роду.
Г. А. Зисман.
У сучасній термодинаміки В. н. т. формулюється єдиним і найбільш загальним чином як закон зростання особливої функції стану системи, яку Клаузіус назвав ентропією (позначається S). Згідно з цим законом, в замкнутій системі ентропія S при будь-якому реальному процесі або зростає, або залишається незмінною, т. Е. Зміна ентропії d S ³ 0; знак рівності має місце для оборотних процесів. У стані рівноваги ентропія замкнутої системи досягає максимуму і ніякі макроскопічні процеси в такій системі, згідно з В. н. т., неможливі. Для незамкненою системи напрямок можливих процесів, а також умови рівноваги можуть бути отримані із закону зростання ентропії, застосованого до складовою замкнутій системі, одержуваної шляхом приєднання всіх тіл, що беруть участь в процесі. Це призводить в загальному випадку необоротних процесів до нерівностей
 d Q £ T dS, (1)
d Q £ T dS, (1)
d U - T dS - d A £ 0, (1 ¢)
де d Q - передане системі кількість теплоти, d А - досконала над нею робота, d U - зміна її внутрішньої енергії, Т - абсолютна температура; знак рівності відноситься до оборотних процесів.
Важливі слідства дає застосування В. н. т. до систем, що знаходяться в фіксованих зовнішніх умовах. Наприклад, для систем з фіксованою температурою і об'ємом нерівність (1 ¢) набуває вигляду d F £ 0, де F = U - TS - вільна енергія системи. Таким чином, в цих умовах напрямок реальних процесів визначається спадання вільної енергії, а стан рівноваги - мінімумом цієї величини (див. потенціали термодинамічні ).
Наведені на початку статті формулювання В. н. т. є приватним наслідком загального закону зростання ентропії.
В. н. т., не дивлячись на свою спільність, не має абсолютного характеру, і відхилення від нього ( флуктуації ) Є цілком закономірними. Прикладами таких флуктуаційних процесів є броунівський рух важких частинок, рівноважний теплове випромінювання нагрітих тіл (в тому числі радіошуми), виникнення зародків нової фази при фазових переходах , Мимовільні флуктуації температури і тиску в рівноважної системі і т.д.
статистична фізика , Побудована на аналізі мікроскопічного механізму явищ, що відбуваються в макроскопічних тілах, і з'ясувала фізичну сутність ентропії, дозволила зрозуміти природу В. н. т., визначити межі його застосовності і усунути позірна суперечність між механічною оборотністю будь-якого, як завгодно складного мікроскопічного процесу і термодинамічної необоротністю процесів в макротела.
Як показує статистична термодинаміка (Л. Больцман , Дж. Гіббс ), Ентропія системи пов'язана зі статистичною вагою Р макроскопічного стану:
S = k ln P (k - Больцмана постійна ). Статистичний вага Р пропорційний числу різних мікроскопічних реалізацій даного стану макроскопічної системи (наприклад, різних розподілів значень координат і імпульсів молекул газу, що відповідають певному значенню енергії, тиску та інших термодинамічних параметрів газу), т. Е. Характеризує як би ступінь неточності мікроскопічного опису макросостоянія. Для замкнутої системи ймовірність термодинамічна W даного макросостоянія пропорційна його статистичному вазі і визначається ентропією системи:
W ~ exp (S / k). (2)
Таким чином, закон зростання ентропії має статистично-імовірнісний характер і виражає постійну тенденцію системи до переходу в більш ймовірне стан. Максимально ймовірним є стан рівноваги; за досить великий проміжок часу будь-яка замкнута система досягає цього стану.
Ентропія є величиною адитивною (див. адитивність ), Вона пропорційна числу частинок в системі. Тому для систем з великим числом частинок навіть саме незначна відносна зміна ентропії, що припадає на одну частинку, істотно змінює її абсолютну величину; зміна ж ентропії, що стоїть в показнику експоненти в ур-ванні (2), призводить до зміни ймовірності даного макросостоянія W в величезне число раз. Саме цей факт є причиною того, що для системи з великим числом частинок слідства В. н. т. практично мають не імовірнісний, а достовірний характер. Вкрай малоймовірні процеси, що супроводжуються скільки-небудь помітним зменшенням ентропії, вимагають настільки величезних часів очікування, що їх реалізація є практично неможливою. У той же час малі частини системи, що містять невелику кількість частинок, відчувають безперервні флуктуації, що супроводжуються лише невеликим абсолютним зміною ентропії. Середні значення частоти і розмірів цих флуктуацій є таким же достовірним наслідком статистичної термодинаміки, як і саме В. н. т.
Проілюструємо сказане прикладом, що дозволяє оцінити масштаби величин, що визначають точність В. н. т. і відхилення від нього. Розглянемо флуктуаційний процес, в результаті якого N частинок, спочатку займають об'єм V, рівний 1 мкм 3 (т. Е. 10-18 м 3), сконцентрується мимовільно в половині цього обсягу. Ставлення статистичних ваг початкового (1) і кінцевого (2) станів:
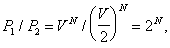
тому зміна ентропії D S / k = N in2 і ставлення ймовірностей W 1 / W 2 = 2 N. Якщо час прольоту частинки через обсяг V, т. Е. Час, протягом якого зберігається дана флуктуація, t = 10-8 сек, то середній час очікування такої флуктуації t = 2 N · t »100,3 N · t. При числі частинок N = 30, t = 10 сек, при N = 100, t »тисячі двадцять дві сек» 1015 років. Якщо ж врахувати, що при атмосферний тиск число часток газу в 1 мкм3 становить N ~ 108, то час очікування вказаної події
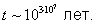
Буквальне застосування В. н. т. до Всесвіту як цілого, що призвело Клаузиуса до неправильного висновку про неминучість «теплової смерті Всесвіту», є неправомірним, так як будь-яка як завгодно велика частина Всесвіту не є сама по собі замкнутої і її наближення до стану теплового рівноваги, навіть не кажучи про флуктуаціях , не є абсолютним.
Термодинамічне ж опис Всесвіту як цілого можливо лише в рамках загальної теорії відносності, в якій висновок про наближення ентропії до максимуму не має місця.
І. М. Ліфшиц.
Літ .: Планк М., Введення в теоретичну фізику, 2 вид., Ч. 5, М. - Л., 1935; Френкель Я. І., Статистична фізика, М. - Л., 1948; Ландау Л., Ліфшиц Е., Статистична фізика, М. - Л., 1951; Леонтович М. А., Введення в термодинаміку, 2 вид., М. - Л., 1952; Самойлович А. Г., Термодинаміка і статистична фізика, М., 1953; Смолуховський М., Межі справедливості другого закону термодинаміки, «Успіхи фізичних наук», 1967, т. 93, ст. 4.